Health Canada poinformowało, że z powodu błędów w dawkowaniu w całym kraju wycofano ze sprzedaży popularny lek przeciwbólowy. Jedna partia butelkowanych kapsułek JAMP-Pregabalin 50 miligramów może przez pomyłkę zawierać kapsułki 150 miligramowe, co może prowadzić do przedawkowania i potencjalnie spowodować poważne lub śmiertelne zagrożenia dla zdrowia.
Dotyczy ona kapsułek JAMP-Pregabalin 50 miligramów o numerze partii 2305012747, numerze identyfikacyjnym leku (DIN) 02435985 i dacie ważności przypadającej na sierpień 2026 r.
JAMP-Pregabalin to lek przeciwbólowy przepisywany dorosłym w celu leczenia bólu spowodowanego uszkodzeniem nerwów spowodowanym cukrzycą, półpaścem lub urazami rdzenia kręgowego. Jest również przepisywany na ból związany z fibromialgią.
Federalne władze ds. zdrowia poinformowały, że przyjęcie zbyt dużej dawki pregabaliny lub nagłe zwiększenie dawki może mieć poważne konsekwencje zagrażające życiu.
„Objawy przedawkowania pregabaliny mogą obejmować: nagłe zmiany nastroju, senność, dezorientację, depresję, pobudzenie, niepokój i drgawki” – informuje Health Canada.
Każdemu, u kogo występują objawy przedawkowania, zaleca się natychmiastową pomoc lekarską.
„Ponadto przyjmowanie zbyt dużej dawki pregabaliny podczas stosowania leków działających na ośrodkowy układ nerwowy, w tym opioidów, wiązało się z problemami z elektryką serca, drgawkami i śmiercią” – czytamy w komunikacie o wycofaniu produktu.
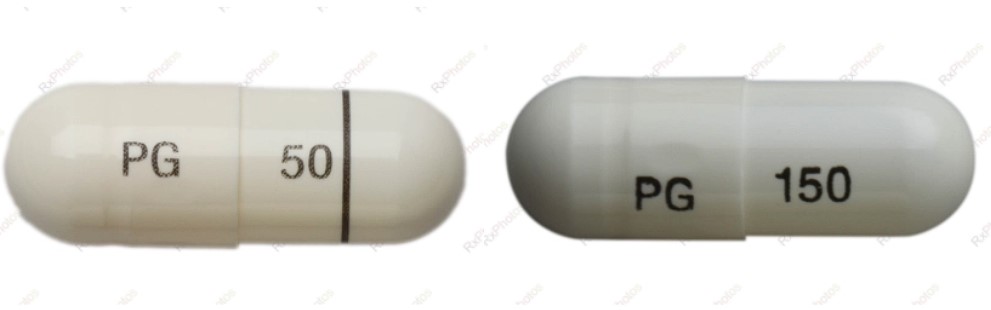
Osobom przyjmującym pregabalinę zaleca się sprawdzenie butelek z lekami, aby upewnić się, że zawierają one wyłącznie kapsułki 50-miligramowe. Kapsułki 50-miligramowe są białe z napisami „PG” i „50” nadrukowanymi czarnym tuszem, natomiast kapsułki 150-miligramowe mają napisy „PG” i „150” nadrukowane czarnym tuszem.
W komunikacie o wycofaniu leku poinformowano, że pacjenci nie powinni nagle przerywać przyjmowania pregabaliny bez wcześniejszej konsultacji z lekarzem, gdyż może to skutkować wystąpieniem objawów odstawienia, takich jak bezsenność, nudności, ból głowy, lęk, nadmierne pocenie się, biegunka i drgawki.
Health Canada poinformowało, że monitoruje wycofanie produktu i zapewni, że producent wdroży działania naprawcze i zapobiegawcze, aby zapobiec wystąpieniu tego problemu w przyszłości.

.jpg)